- HOME
- 本プログラムについて
- ターゲットタンパク研究「食品・環境等の産業利用」分野
- 薬剤排出トランスポート・マシーナリー
多剤耐性化の克服を目指した薬剤排出トランスポート・マシーナリーの構造生物学
代表機関:東京工業大学大学院生命理工学研究科
代表研究者:村上 聡
2010年版パンフレット(背景と成果)の該当ページはこちら
薬剤を使った化学療法は、病原性細菌やがん細胞そのものを排除でき、病気を原因から絶つ治療として重要です。しかし、近年、病原性細菌やがん細胞に薬が効かなくなる“薬剤耐性化”という現象が医療現場の脅威となっています。特に、病院内で抵抗力の低下した患者たちが感染症を起こす院内感染は大きな問題です。
薬が効かなくなるおもな原因は、病原性細菌やがん細胞にある多剤排出トランスポーターが薬剤を排出するためです。多剤排出トランスポーターは細胞膜にあるタンパク質で、細菌からヒトに至る多くの生物に共通に存在し、薬剤や毒物などの異物を細胞の外に送り出すはたらきをします。
一般に、細胞ではたらくタンパク質は、決められた相手にしか作用しないという性質があります。しかし、多剤排出トランスポーターは例外的に、いろいろな薬剤を認識して排出します。そのため、多くの薬剤が効かない“多剤耐性”という現象が起こるのです。
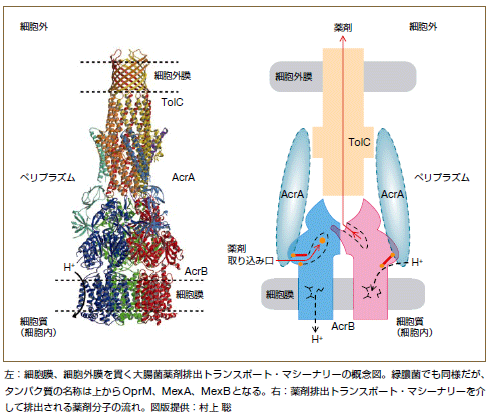
細菌の中でも、大腸菌、緑膿菌などのグラム陰性菌は、細胞膜の外側に細胞外膜というもう1枚の膜をもっています。このため、薬剤の排出は、細胞膜にある多剤排出トランスポーター(AcrBやMexB)と、細胞外膜にある外膜チャンネル(TolCやOprM)、そして両者をつなぐアダプター(AcrAやMexA)の3種類のタンパク質からできた複合体(トランスポート・マシーナリー)が行っています。
私たちのグループは、2002年に大腸菌の多剤排出トランスポーターの結晶構造解析に成功しました。これは世界で初めてのことで注目を浴びました。また、2006年には、このトランスポーターと薬剤が結合した状態での構造も決定し、多剤排出のメカニズム解明に向けて一歩前進しました。また、分担研究者である北里大学基礎研究所の中江太治博士のグループは、緑膿菌の外膜チャネルとアダプターの構造を決定しています。
残された課題は、実際に機能している状態のトランスポート・マシーナリーの全体構造を明らかにすることと、さまざまな病原性細菌のもつ多剤排出トランスポーターのはたらきを詳細な立体構造に基づいて解明することです。私たちはこの課題に取り組み、得られた情報は、トランスポート・マシーナリーによる薬剤排出を阻害する薬や、排出されずに細菌内にとどまり効果を発揮する薬など、多剤耐性化問題を解決してくれる特効薬の開発につなげたいと考えています。

 サイト内検索
サイト内検索